Алесио Ненсиони, Ирен Кафа, Салваторе Кортелино
Резюме | Уязвимостта на раковите клетки към недостиг на хранителни вещества и тяхната зависимост от специфични метаболити са нововъзникващи отличителни белези на рака. Диетите на гладно или имитиращи гладуване (FMDs) водят до широки промени в растежните фактори и нивата на метаболитите, създавайки среда, която може да намали способността на раковите клетки да се адаптират и оцеляват и по този начин да подобрят ефектите от терапиите за рак. В допълнение, гладуването или FMD повишават резистентността към химиотерапия в нормалните, но не и раковите клетки и насърчават регенерацията в нормалните тъкани, което може да помогне за предотвратяване на вредни и потенциално животозастрашаващи странични ефекти от лечението. Докато гладуването трудно се понася от пациентите, както животинските, така и клиничните проучвания показват, че циклите на нискокалорични шап са осъществими и като цяло безопасни. Няколко клинични проучвания, оценяващи ефекта на гладуване или шап върху нежеланите събития, свързани с лечението, и върху резултатите от ефикасността са в ход. Ние предлагаме комбинацията от шап с химиотерапия, имунотерапия или други лечения да представлява потенциално обещаваща стратегия за повишаване на ефикасността на лечението, предотвратяване на придобиване на резистентност и намаляване на страничните ефекти.
Факторите, свързани с храненето и начина на живот, са ключови детерминанти на риска от развитие на рак, като някои видове рак са по-зависими от хранителните навици, отколкото други1
Въпреки че през последното десетилетие станахме свидетели на безпрецедентни промени и забележителен напредък в лечението на рака14,15, остава съществена нужда от по-ефективни и вероятно,
Гладуването принуждава здравите клетки да влязат в бавно делене и силно защитен режим, който ги предпазва от токсични обиди, получени от противоракови лекарства, като същевременно сенсибилизира различни видове ракови клетки към тези терапевтични средства11,12,17. Това откритие предполага, че една единствена диетична интервенция може потенциално да помогне за справяне с различни и еднакво важни аспекти на терапията на рака.
В тази статия на Становището обсъждаме биологичната обосновка за използването на диети на гладно или имитиращи гладуване (FMDs) за притъпяване на TEAE, но също и за предотвратяване и лечение на рак. Ние също така илюстрираме предупрежденията на този експериментален подход18,19 и публикуваните и текущи клинични проучвания, в които гладуването или FMD са били прилагани при пациенти с рак.
Съдържание
Системен и клетъчен отговор на гладуване
Гладуването води до промени в активността на много метаболитни пътища, свързани с преминаването към режим, способен да генерира енергия и метаболити, използвайки въглеродни източници, освободени предимно от мастната тъкан и отчасти от мускулите. Промените в нивата на циркулиращите хормони и метаболити се превръщат в намаляване на клетъчното делене и метаболитна активност на нормални клетки и в крайна сметка да ги предпази от химиотерапевтични инсулти11,12. Раковите клетки, като не се подчиняват на заповедите срещу растежа, продиктувани от тези условия на глад, могат да имат обратен отговор на нормалните клетки и следователно да станат чувствителни към химиотерапия и други терапии за рак.
Системен отговор на гладуване
Отговорът на гладуването е организиран отчасти от циркулиращите нива на глюкоза, инсулин, глюкагон, растежен хормон (GH), IGF1, глюкокортикоиди
Глюкагонът и ниските нива на инсулин също стимулират разграждането на триглицеридите (които най-вече се съхраняват в мастната тъкан) до глицерол и свободни мастни киселини. По време на гладуване повечето тъкани използват мастни киселини за енергия, докато мозъкът разчита на глюкоза и кетонни тела, произведени от хепатоцити (кетонните тела могат да се произвеждат от ацетил-КоА, генериран от α-окислението на мастни киселини или от кетогенни аминокиселини). В кетогенната фаза на гладуване, кетонните тела достигат концентрации в милимоларния диапазон, обикновено започвайки след 2 дни от началото на гладуването. Заедно с глицерол и аминокиселини, извлечени от мазнини, кетонните тела захранват глюконеогенезата, която поддържа нивата на глюкоза при концентрация от приблизително 3 mM (4 mg на dl), която се използва най-вече от мозъка.
Глюкокортикоидите и адреналинът също допринасят за насочването на метаболитните адаптации към
И накрая, гладуването намалява нивата на циркулиращия лептин, хормон, произвеждан предимно от адипоцити, който инхибира глада, като същевременно повишава нивата на адипонектин, който увеличава разграждането на мастни киселини23,24. По този начин, в заключение, отличителните белези на системния отговор на бозайниците към гладуване са ниски нива на глюкоза и инсулин, високи нива на глюкагон и кетонни тела, ниски нива на IGF1 и лептин и високи нива на адипонектин.
Клетъчен отговор на гладуване
Реакцията на здравите клетки към гладуването е еволюционно запазена и осигурява клетъчна защита, а поне в моделните организми е доказано, че увеличава продължителността на живота и здравето12,22,25. IGF31
Гладуването и произтичащото от него ограничаване на глюкозата инхибират активността на PKA, повишават активността на AMPK и активират EGR1 и по този начин постигат клетъчно-протективни ефекти, включително тези в миокарда22,25,26. И накрая, гладуването и FMDs (вижте по-долу за техния състав) също имат способността да насърчават регенеративните ефекти (Каре 1) чрез молекулярни механизми, някои от които са замесени в рак, като повишена аутофагия или индукция на активност на сиртуин22,37 49 .

Диетични подходи при ракови шап
Диетичните подходи, базирани на гладуване, които са изследвани по-обстойно в онкологията, както предклинично, така и клинично, включват гладуване на вода (въздържане от всякакви храни и напитки с изключение на вода) и FMDs11,12,17,25,26,50 60 (Таблица 1). Предварителните клинични данни показват, че може да е необходимо гладуване от най-малко 48 часа за постигане на клинично значими ефекти в онкологията, като например предотвратяване на увреждане на ДНК, предизвикано от химиотерапия, на здрави тъкани и подпомагане на поддържането
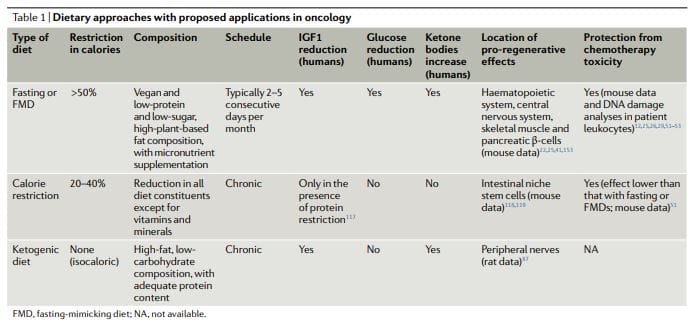
Въпреки това, повечето пациенти отказват или изпитват затруднения да завършат гладуването с вода, а потенциалните рискове от удължения дефицит на калории и микроелементи, свързани с него, са трудни за оправдаване. FMDs са медицински разработени диетични режими с много ниско съдържание на калории (тоест обикновено между 300 и 1,100 kcal на ден), захари и протеини, които пресъздават много от ефектите на гладуването само с вода, но с по-добро спазване на пациентите и намален хранителен риск22,61,62, 3. По време на FMD пациентите обикновено получават неограничени количества вода, малки, стандартизирани порции зеленчукови бульони, супи, сокове, ядки и билкови чайове, както и добавки от микроелементи. В клинично проучване на 5 месечни цикъла на 1-дневна FMD при общо здрави индивиди, диетата се понася добре и намалява телесните мазнини, кръвното налягане и нивата на IGF62. В предишни и текущи онкологични клинични изпитвания, гладуването или FMD обикновено са били прилагани на всеки 3 седмици, например, в комбинация с режими на химиотерапия, като продължителността им е варирала между 4 и 1 дни5 . Важно е, че в това проучване не са докладвани сериозни нежелани събития (ниво G52,53,58,61,63 или по-високо, съгласно Общите терминологични критерии за нежелани събития)68.
Кетогенни диети
Кетогенните диети (КД) са диетични режими, които имат нормално калорично, високо съдържание на мазнини и ниско съдържание на въглехидрати69,70. При класическата KD съотношението между теглото на мазнините и комбинираното тегло на въглехидратите и протеините е 4:1. Трябва да се отбележи, че FMDs също са кетогенни, тъй като имат високо съдържание на мазнини и имат способността да предизвикват значително повишаване (?0.5 mmol на литър) в нивата на циркулиращите кетонни тела. При хората KD може също да намали нивата на IGF1 и инсулин (с повече от 20% от изходните стойности), въпреки че тези ефекти се влияят от нивата и видовете въглехидрати и протеини в диетата71. KD могат да намалят нивата на кръвната захар, но те обикновено остават в нормалните граници (тоест >4.4 mmol на литър)71.
По-специално, KDs могат да бъдат ефективни за предотвратяване на повишаването на глюкозата и инсулина, което обикновено се появява в отговор на PI3K инхибитори, което се предлага да ограничи тяхната ефикасност72. Традиционно KD се използват за лечение на рефрактерна епилепсия, главно при деца69. При миши модели KDs предизвикват противоракови ефекти, особено при глиобластома70,72. Клиничните проучвания показват, че KD вероятно нямат значителна терапевтична активност, когато се използват като единични агенти при пациенти с рак и предполагат, че потенциалните ползи от тези диети трябва да се търсят в комбинация с други подходи, като химиотерапия, лъчетерапия, антиангиогенни лечения, PI86K инхибитори
Съобщава се, че KD имат невропротективни ефекти в периферните нерви и в хипокампуса87,88. Остава обаче да се установи дали KDs също имат прорегенеративни ефекти, подобни на гладуването или FMDs (Каре 1) и дали KDs също могат да се използват за защита на живи бозайници от токсичността на химиотерапията. По-специално, регенеративните ефекти на гладуването или FMD изглежда се максимизират чрез превключване от режима на реакция на глад, който включва разпадането на клетъчните компоненти и смъртта на много клетки, и периода на повторно хранене, в който клетките и тъканите се подлагат на реконструкция 22. Тъй като KD не принуждават влизането в режим на гладуване, не насърчават голямо разпадане на вътреклетъчните компоненти и тъкани и не включват период на повторно захранване, е малко вероятно те да причинят типа координирана регенерация, наблюдавана по време на повторното хранене на шап.
Ограничение на калориите
Докато хроничното ограничаване на калориите (CR) и диетите с дефицит на специфични аминокиселини са много различни от периодичното гладуване, те споделят с гладуването и шап повече или по-малко селективно ограничение на хранителните вещества и имат противоракови ефекти81,89. CR обикновено включва хронично намаляване с 112% на енергийния прием от стандартния прием на калории, което би позволило на индивида да поддържа нормално тегло20. Той е много ефективен за намаляване на сърдечносъдовите рискови фактори и заболеваемостта от рак при моделни организми, включително примати30.
Въпреки това, CR може да причини странични ефекти, като промени във външния вид, повишена чувствителност към студ, намалена сила, менструални нередности, безплодие, загуба на либидо, остеопороза, по-бавно зарастване на рани, мания за храна, раздразнителност и депресия. При пациенти с рак има сериозни опасения, че това може да влоши недохранването и че неизбежно ще причини прекомерна загуба на чиста телесна маса18,113 116. CR намалява нивата на кръвната захар на гладно, въпреки че те остават в нормалните граници114. При хората хроничният CR не влияе на нивата на IGF1, освен ако не се приложи умерено протеиново ограничение117.
Проучванията показват, че чрез намаляване на сигнализирането на mTORC1 в клетките на Paneth, CR увеличава тяхната функция на стволови клетки и че също така защитава резервните чревни стволови клетки от увреждане на ДНК118,119, но не е известно дали про-регенеративните ефекти в други органи също се предизвикват от CR. По този начин наличните данни предполагат, че гладуването и FMD създават метаболитен, регенеративен и защитен профил, който е различен и вероятно по-мощен от този, предизвикан от KD или CR.
Гладене и шап в терапията: Ефекти върху нивата на хормони и метаболити
Много от промените в нивата на циркулиращите хормони и метаболити, които обикновено се наблюдават в отговор на гладуване, имат способността да упражняват противотуморни ефекти (тоест намалени нива на глюкоза, IGF1, инсулин и лептин и повишени нива на адипонектин)23,120,121 и/ или да осигури защита на здравите тъкани от странични ефекти (тоест, намалени нива на IGF1 и глюкоза). Тъй като кетонните тела могат да инхибират хистон деацетилази (HDACs), индуцираното от гладуване увеличение на кетонните тела може да помогне за забавяне на растежа на тумора и да насърчи диференциацията чрез епигенетични механизми122.
Доказано е обаче, че ацетоацетатът на кетонното тяло ускорява, вместо да намалява, растежа на някои тумори, като меланоми с мутирал BRAF123. Тези промени, за които има най-силни доказателства за роля в благоприятните ефекти на гладуването и шап срещу рак, са намаляването на нивата на IGF1 и глюкозата. На молекулярно ниво гладуването или FMD намаляват вътреклетъчните сигнални каскади, включително IGF1R AKT mTOR S6K и cAMP PKA сигнализиране, повишава аутофагията, помага на нормалните клетки да издържат на стрес и насърчава противораковия имунитет25,29,56,124
Диференциална устойчивост на стрес: Увеличаване на поносимостта към химиотерапия
Някои онкогенни ортолози на дрожди, като Ras и Sch9 (функционален ортолог на S6K на бозайници), са в състояние да намалят устойчивостта на стрес в моделните организми27,28. В допълнение, мутации, които активират IGF1R, RAS, PI3KCA или AKT, или които инактивират PTEN, присъстват в по-голямата част от човешките ракови заболявания10. Заедно това доведе до хипотезата, че гладуването ще причини противоположни ефекти при рак спрямо нормалните клетки по отношение на способността им да издържат на клетъчни стресори, включително химиотерапевтици. С други думи, гладуването може да доведе до
Според хипотезата на DSR, нормалните клетки реагират на гладуване чрез понижаване на пролиферацията, свързана с рибозомната биогенеза и/или гените за сглобяване, което принуждава клетките да влязат в режим на самоподдържане и ги предпазва от щетите, причинени от химиотерапия, лъчетерапия и други токсични агенти. Обратно, в раковите клетки този режим на самоподдържане се предотвратява чрез онкогенни промени, които причиняват конститутивно инхибиране на пътищата за реакция на стрес12 (Фиг. 1). В съответствие с модела DSR, краткосрочно гладуване или изтриване на протоонкоген
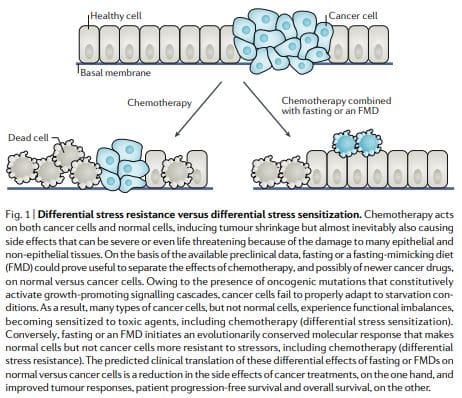
Подобни резултати са получени при клетки от бозайници: излагането на среда с ниско съдържание на глюкоза защитава първичните миши глия клетки срещу токсичност от водороден пероксид или циклофосфамид (прооксидантно химиотерапевтично средство), но не защитава миши, плъхове и човешки ракови клетъчни линии на глиома и невробластома. В съответствие с тези наблюдения,
Последващи проучвания установяват, че намалената сигнализация на IGF1 в отговор на гладуване защитава първичната глия и невроните, но не и клетките на глиома и невробластома, от циклофосфамид и от прооксидативни съединения и защитава миши ембрионални фибробласти от доксорубицин29. Мишки с чернодробен дефицит на IGF1 (LID), трансгенни животни с условна делеция на чернодробния Igf1 ген, които показват 70% намаление на циркулиращите нива на IGF80 (нива, подобни на тези, постигнати при 1-часово гладуване при мишки)72, бяха защитени срещу три от четири тествани химиотерапевтични лекарства, включително доксорубицин.
Хистологичните проучвания показват признаци на индуцирана от доксорубицин сърдечна миопатия само при третирани с доксорубицин контролни мишки, но не и при мишки LID. При експерименти с животни, носещи меланом, лекувани с доксорубицин, не се наблюдава разлика по отношение на прогресията на заболяването между контролни и LID мишки, което показва, че раковите клетки не са защитени от химиотерапия чрез намалени нива на IGF1. И все пак, отново, носещи тумори LID мишки показват забележително предимство в оцеляването в сравнение с контролните животни поради способността им да издържат на токсичността на доксорубицин29. По този начин, като цяло, тези резултати потвърждават, че понижаването на IGF1 е ключов механизъм, чрез който гладуването повишава поносимостта на химиотерапията.
Както дексаметазонът, така и инхибиторите на mTOR се използват широко при лечение на рак, било поради тяхната ефикасност като антиеметици и
Тези интервенции намаляват активността на PKA, като същевременно повишават активността на AMPK и по този начин активират EGR1, което показва, че cAMP PKA сигнализирането медиира предизвикания от гладно DSR чрез EGR1 (реф. 26). EGR1 също така насърчава експресията на кардиопротективни пептиди, като предсърдния натриуретичен пептид (ANP) и В-тип натриуретичен пептид (BNP) в сърдечната тъкан, което допринася за резистентността към доксорубицин. Освен това, гладуването и/или FMD могат да предпазят мишките от индуцирана от доксорубицин кардиомиопатия чрез засилване на аутофагията, което може да насърчи клетъчното здраве чрез намаляване на производството на реактивни кислородни видове (ROS) чрез елиминиране на дисфункционални митохондрии и чрез отстраняване на токсични агрегати.
В допълнение към намаляването на индуцирана от химиотерапия токсичност в клетките и увеличаване на преживяемостта на мишки, лекувани с химиотерапия, циклите на гладуване предизвикват регенерация на костния мозък и предотвратяват имуносупресията, причинена от циклофосфамид по PKA-свързан и свързан с IGF1 начин25. По този начин убедителните предклинични резултати показват потенциала на гладуването и FMD да повишат поносимостта на химиотерапията и да избегнат големи странични ефекти. Тъй като първоначалните клинични данни дават допълнителна подкрепа на този потенциал, тези предклинични проучвания изграждат силна обосновка за оценка на шап в рандомизирани клинични проучвания с TEAEs като първична крайна точка.
Диференциална чувствителност към стрес: Увеличаване на смъртта на раковите клетки
Ако се използват самостоятелно, повечето диетични интервенции, включително гладуване и шап, имат ограничен ефект срещу прогресията на рака. Според хипотезата за диференциална стрес-сенсибилизация (DSS), комбинацията от гладуване или шап с второ лечение е много по-обещаваща11,12. Тази хипотеза предвижда, че докато раковите клетки са в състояние да се адаптират към ограничени концентрации на кислород и хранителни вещества, много видове ракови клетки не са в състояние да извършат промени, които биха позволили оцеляване в токсична среда с дефицит на хранителни вещества, генерирана от комбинацията от гладуване и химиотерапия , например. Ранни експерименти при рак на гърдата, меланом
Ние считаме такъв неподходящ отговор на раковите клетки към променените състояния, включително намаляването на нивата на IGF1 и глюкозата, причинени от гладуване или шап, като ключов механизъм, лежащ в основата на

Чрез намаляване на наличността на глюкоза и увеличаване на ?-окислението на мастни киселини, гладуването или FMD могат също да насърчат преминаването от аеробна гликолиза (ефект на Warburg) към митохондриално окислително фосфорилиране в раковите клетки, което е необходимо за поддържане на растежа на раковите клетки в най-бедната на хранителни вещества среда50 (фиг. 2). Това превключване води до повишено производство на ROS11 в резултат на повишена митохондриална респираторна активност и може също да включва намаляване на клетъчния редокс потенциал поради намаления синтез на глутатион от гликолизата и пътя на пентозофосфата50. Комбинираният ефект от увеличаването на ROS и намалената антиоксидантна защита повишава оксидативния стрес в раковите клетки и усилва активността на химиотерапевтиците. По-специално, тъй като високата гликолитична активност, демонстрирана от производството на високо лактат, е предсказваща агресивността и метастатичната склонност при няколко вида рак129, анти-Warburg ефектите на гладуването или FMD имат потенциала да бъдат особено ефективни срещу агресивни и метастатични ракови заболявания.
Освен промяна в метаболизма, гладуването или FMD предизвикват други промени, които могат да насърчат DSS в раковите клетки на панкреаса. Гладуването повишава нивата на експресия на
И накрая, гладуването може да регулира нагоре рецептора на лептин и надолу по веригата
По-специално, вероятно е много видове ракови клетки, включително AML29, да придобият резистентност чрез заобикаляне на метаболитните промени, наложени от гладуване или FMD, възможност, която допълнително се увеличава от метаболитната хетерогенност, която характеризира много видове рак129. По този начин основна цел в близко бъдеще ще бъде да се идентифицират видовете рак, които са най-податливи на тези диетични режими с помощта на биомаркери. От друга страна, когато се комбинират със стандартни терапии, гладуването или FMD рядко водят до придобиване на резистентност при ракови миши модели, а резистентността към гладуване, комбинирана с химиотерапия, също е необичайна в проучвания in vitro, подчертавайки важността на идентифицирането на терапии, които, когато се комбинира с FMDs, води до мощни токсични ефекти срещу ракови клетки с минимална токсичност за нормалните клетки и тъкани11,17,50,55 57,59,124.
Повишаване на противотуморния имунитет чрез гладуване или FMD
Последните данни показват, че гладуването или FMD сами по себе си и в по-голяма степен, когато се комбинират с химиотерапия, предизвикват разширяване на лимфоидните прогенитори и насърчават
Противоракови диети при миши модели
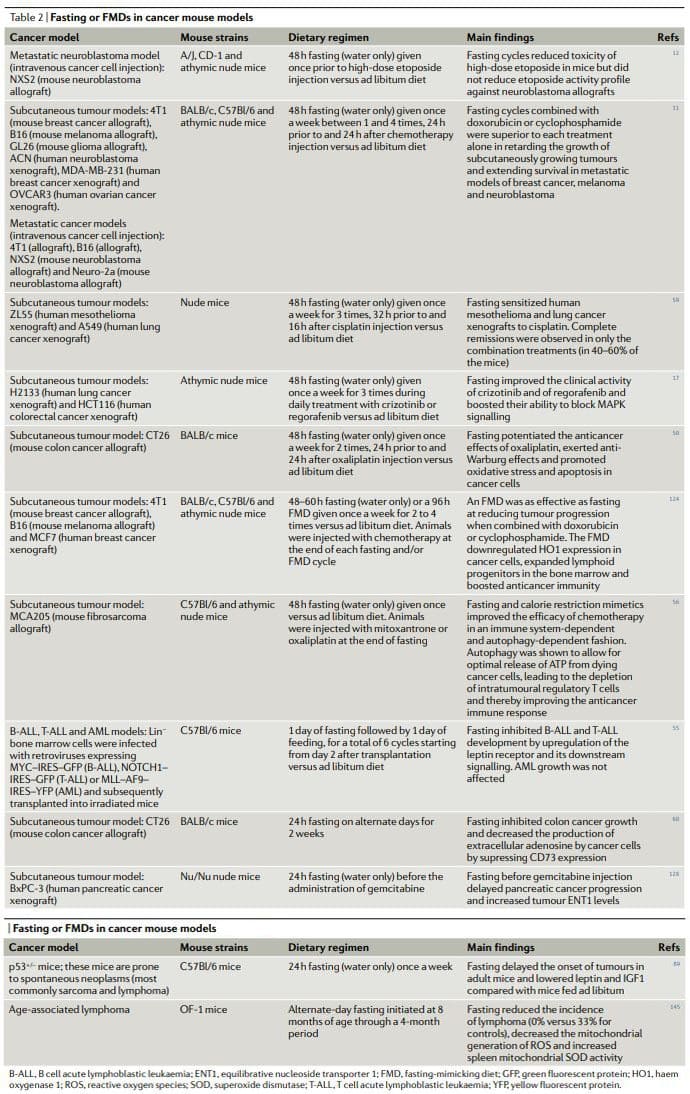
Като цяло, резултатите от предклиничните проучвания на гладуване или FMDs в модели на рак при животни, включително модели за метастатичен рак (Таблица 2), показват, че периодичното гладуване или FMDs постигат плейотропни противоракови ефекти и потенцират активността на химиотерапевтиците и TKI, като същевременно упражняват защитни и регенеративни ефекти в множество органи22,25. Постигането на същите ефекти без гладуване и/или шап би изисквало първо идентифициране и след това употребата на множество ефективни, скъпи и често токсични лекарства и вероятно няма да има предимството да предизвика здрава клетъчна защита. Трябва да се отбележи, че в поне две проучвания гладуването, комбинирано с химиотерапия, се оказа единствената интервенция, способна да постигне или пълна регресия на тумора, или дългосрочно оцеляване при постоянна част от лекуваните животни11,59
Хроничните KD също показват a
CR намалява туморогенезата при генетични миши модели на рак, миши модели със спонтанна туморогенеза и канцерогенно индуцирани ракови мишки модели, както и при маймуни91,92,97,98,101,102,104 106,108,109,136 138. Обратно, проучване установи, че CR от средна възраст действително увеличава честотата на неоплазмите на плазмените клетки при C57Bl/6 мишки139. Въпреки това, в същото проучване, CR също удължава максималната продължителност на живота с приблизително 15%, а наблюдаваното увеличение на заболеваемостта от рак се дължи на увеличената продължителност на живота на мишките, подложени на CR, възрастта, на която
Важно е, че CR подобри активността на противораково лечение в няколко модела на рак, включително активността на антиIGF1R антитяло (ганитумаб) срещу рак на простатата141, циклофосфамид срещу клетки на невробластома135 и инхибиране на аутофагията в ксенотрансплантатите на HRAS-G12V, трансформирани безсмъртни клетки на бебето, епидемична мишка. Въпреки това, CR или KD в комбинация с противоракови терапии изглежда са по-малко ефективни от гладуването. Проучване при мишки установи, че за разлика от самото гладуване, само CR не е в състояние да намали растежа на подкожно растящи GL100 миши глиоми и че отново, за разлика от краткосрочното гладуване, CR не повишава активността на цисплатина срещу подкожната 26T4 гърда тумори1. В същото проучване гладуването също се оказа значително по-ефективно от CR и KD за повишаване на поносимостта на доксорубицин51. Въпреки че гладуването или FMD, CR и KD вероятно действат и модулират припокриването
Фазата на повторно захранване може тогава
Гладене и шап в превенцията на рака
Епидемиологични проучвания и проучвания при животни, включително маймуни108,109,144, и хора подкрепят схващането, че хроничният CR и периодичното гладуване и/или шап могат да имат превантивни ефекти при хората. Независимо от това, CR трудно може да се приложи в общата популация поради проблеми със спазването и възможни странични ефекти115. По този начин, докато основани на доказателства препоръки за храни, които трябва да се предпочитат (или да се избягват), както и препоръки за начина на живот за намаляване на риска от рак се утвърждават6,8,9,15, целта сега е да се идентифицират и евентуално да се стандартизират добре поносимите, периодични диетични режими с ниски или никакви странични ефекти и оценяват тяхната ефикасност за превенция на рак в клинични проучвания.
Както беше обсъдено по-рано, циклите на FMD причиняват понижаване на IGF1 и глюкозата и повишаване на IGFBP1 и кетонни тела, които са промени, подобни на тези, причинени от самото гладуване и са биомаркери на реакцията на гладно22. Когато C57Bl/6 мишки (които спонтанно се развиват
Предишно проучване на алтернативно гладуване, което е проведено при мишки на средна възраст за общо 4 месеца, също установи, че гладуването намалява честотата на лимфома, като я довежда от 33% (за контролни мишки) до 0% (при гладуващи животни)145, въпреки че поради кратката продължителност на изследването не е известно дали този режим на гладуване предотвратява или просто забавя
Следователно, обещаващите резултати от предклинични проучвания, комбинирани с клиничните данни за ефекта на шап върху рисковите фактори за
Клинична приложимост в онкологията
Към днешна дата са публикувани четири проучвания за осъществимост на гладуване и шап при пациенти, подложени на химиотерапия52,53,58,61. В серия от случаи от 10 пациенти, диагностицирани с различни видове рак, включително рак на гърдата, простатата, яйчниците, матката, белия дроб и рак на хранопровода, които доброволно гладуват до 140 часа преди и/или до 56 часа след химиотерапията, не са причинени сериозни странични ефекти самото гладуване, освен глад и замаяност, са докладвани58. Тези пациенти (шест), които са били подложени на химиотерапия с и без гладуване, съобщават за значително намаляване на умората, слабостта и стомашно-чревните нежелани събития по време на гладуване. В допълнение, при тези пациенти, при които прогресията на рака може да бъде оценена, гладуването не предотвратява предизвикано от химиотерапия намаляване на туморния обем или на туморните маркери. В друго проучване 13 жени с HER2 (известен също като ERBB2) отрицателен, стадий II/III рак на гърдата, получаващи неоадювантна химиотерапия с таксотер, адриамицин и циклофосфамид (TAC), бяха рандомизирани на бърза (само вода) 24 часа преди и след началото на химиотерапията или на хранене според стандартните насоки52.
Краткосрочното гладуване се понася добре и намалява спада на средния брой еритроцити и тромбоцити 7 дни след химиотерапията. Интересно е, че в това проучване нивата на ?-H2AX (маркер за увреждане на ДНК) се повишават 30 минути след химиотерапия в левкоцити от пациенти, които не са гладували, но не и при пациенти, които са гладували. При повишаване на дозата на гладуване при пациенти, подложени на химиотерапия на базата на платина, 20 пациенти (които са лекувани основно за рак на уротелия, яйчниците или гърдата) бяха рандомизирани да гладуват за 24, 48 или 72 часа (разделени на 48 часа преди химиотерапията и 24 часа след химиотерапията )53. Критериите за осъществимост (дефинирани като три или повече от шест субекта във всяка кохорта, консумиращи?200 kcal на ден по време на бързия период без излишна токсичност) бяха изпълнени. Токсичности, свързани с гладуване
Съвсем наскоро беше проведено рандомизирано кръстосано клинично проучване, оценяващо ефектите на шап върху качеството на живот и страничните ефекти от химиотерапията при общо 34 пациенти с рак на гърдата или яйчниците61. FMD се състоеше от
Предизвикателства в клиниката
Изследването на периодично гладуване или на шап в онкологията не е лишено от опасения, особено във връзка с възможността този тип диетичен режим да предизвика недохранване, саркопения,
Заключения
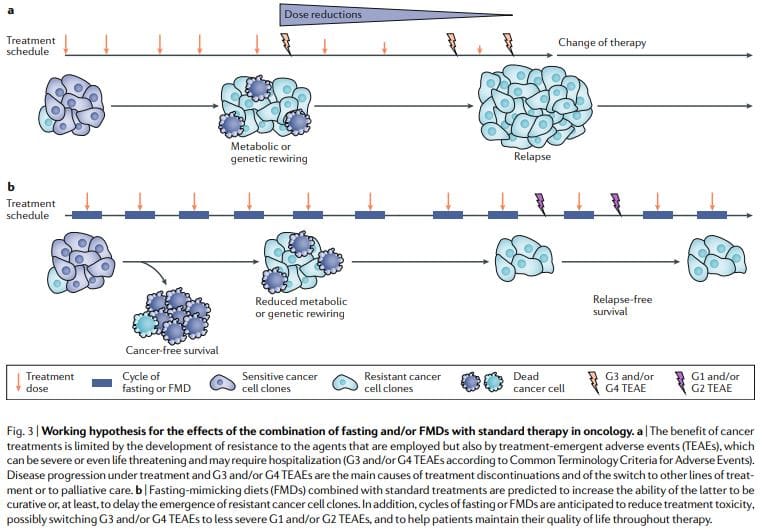
Периодичното гладуване или FMD постоянно показват мощни противоракови ефекти при модели на рак при мишки, включително способността да се потенцира химиорадиотерапията и TKI и да се задейства противораков имунитет. Циклите на шап са по-осъществими от хроничните диетични режими, тъй като позволяват на пациентите да консумират храна редовно по време на шап, да поддържат нормална диета между циклите и не водят до тежка загуба на тегло и евентуално вредни ефекти върху имунната и ендокринната система. По-специално, като самостоятелни терапии, периодичното гладуване или циклите на FMD вероятно биха показали ограничена ефикасност срещу установени тумори. Всъщност при мишки гладуването или шапата влияят върху прогресията на редица видове рак подобно на химиотерапията, но сами по себе си те рядко съответстват на ефекта, получен в комбинация с лекарства за рак, което може да доведе до оцеляване без рак11,59. По този начин, ние предлагаме комбинацията от периодични цикли на шап със стандартни лечения да притежава най-висок потенциал за насърчаване на оцеляването без рак при пациенти, както е предложено от миши модели11,59 (Фиг. 3).
Тази комбинация може да бъде особено мощна поради няколко причини: първо, лекарствата за рак и други терапии могат да бъдат ефективни, но част от пациентите не реагират, защото раковите клетки приемат алтернативни метаболитни стратегии, водещи до оцеляване. Тези алтернативни метаболитни режими са много по-трудни за поддържане при условия на гладуване или шап поради дефицитите или промените в глюкозата, някои аминокиселини, хормони и растежни фактори, както и в други неизвестни пътища, водещи до клетъчна смърт. Второ, гладуването или FMD могат да предотвратят или намалят придобиването на резистентност. Трето, гладуването или FMD защитават нормалните клетки и органи от страничните ефекти, причинени от голямо разнообразие от лекарства за рак. Въз основа на предклинични и клинични доказателства за приложимост, безопасност и ефикасност (при намаляване на IGF1, висцерална мазнина
Освен това е важно да се прилагат шап с разбиране на механизмите на действие, тъй като ефикасността им
Текущите клинични проучвания на шап при пациенти с рак63,65 ще дадат по-солидни отговори дали предписването на периодични шап в комбинация с конвенционални противоракови средства помага за подобряване на поносимостта и активността на последните. Важно е да се има предвид, че FMD няма да бъдат ефективни за намаляване на страничните ефекти от лечението на рак при всички пациенти и няма да работят за подобряване на ефикасността на всички терапии, но имат голям потенциал да направят това поне за част и евентуално за голяма част от пациентите и лекарства. Немощни или недохранени пациенти или пациенти с риск от недохранване не трябва да бъдат включени в клинични проучвания на гладуване или шап, а хранителният статус на пациентите и анорексията трябва да бъдат внимателно наблюдавани по време на клиничните изпитвания.
Литература:
Професионален обхват на практика *
Информацията тук на "Гладене и рак: молекулярни механизми и клинично приложение" няма за цел да замени личната връзка с квалифициран здравен специалист или лицензиран лекар и не е медицински съвет. Насърчаваме ви да вземате здравни решения въз основа на вашите изследвания и партньорство с квалифициран здравен специалист.
Информация за блога и дискусии за обхват
Нашият информационен обхват е ограничено до хиропрактика, мускулно-скелетни, физически лекарства, уелнес, допринасящи етиологични висцерозоматични нарушения в рамките на клинични презентации, свързана соматовисцерална рефлексна клинична динамика, сублуксационни комплекси, чувствителни здравни проблеми и/или статии, теми и дискусии от функционална медицина.
Ние предоставяме и представяме клинично сътрудничество със специалисти от различни дисциплини. Всеки специалист се ръководи от своя професионален обхват на практика и своята юрисдикция за лицензиране. Използваме протоколи за функционално здраве и уелнес за лечение и поддържане на грижи за наранявания или нарушения на мускулно-скелетната система.
Нашите видеоклипове, публикации, теми, теми и прозрения обхващат клинични въпроси, проблеми и теми, които се отнасят до и пряко или косвено подкрепят нашия клиничен обхват на практика.*
Нашият офис разумно се е опитал да предостави подкрепящи цитати и е идентифицирал съответното научно изследване или проучвания, подкрепящи нашите публикации. Ние предоставяме копия на подкрепящи научни изследвания, достъпни за регулаторните съвети и обществеността при поискване.
Разбираме, че обхващаме въпроси, които изискват допълнително обяснение как може да подпомогне определен план за грижи или протокол за лечение; следователно, за да обсъдите допълнително темата по-горе, моля не се колебайте да попитате Д-р Алекс Хименес, окръг Колумбия, Или се свържете с нас на адрес 915-850-0900.
Ние сме тук, за да помогнем на вас и вашето семейство.
Благословения
Д-р Алекс Хименес н.е., MSACP, RN*, CCST, IFMCP*, CIFM*, ATN*
имейл: coach@elpasofunctionalmedicine.com
Лицензиран като доктор по хиропрактика (DC) в Тексас & Ню Мексико*
Тексас DC Лиценз # TX5807, Ню Мексико DC Лиценз # NM-DC2182
Лицензирана като регистрирана медицинска сестра (RN*) in Флорида
Флорида Лиценз RN Лиценз # RN9617241 (Контролен номер 3558029)
Компактен статус: Многодържавен лиценз: Упълномощен да практикува в 40 състояния*
Д-р Алекс Хименес DC, MSACP, RN* CIFM*, IFMCP*, ATN*, CCST
Моята цифрова визитка